Antibiotikaresistens og ny behandling mot tuberkulose
Tuberkulose (TB) er en alvorlig global sykdom som forverres ytterligere med økende antibiotikaresistens. Det er et stort behov for nye medikamenter i behandlingen av TB. Det må til for å nå bærekraftsmålet om å utrydde TB innen 2030.
Tekst av: Tahira Riaz, postdoktor, UiO, Pål Rongved, professor, UiO, Marta Gómez-Muñoz, PhD student UiO / TTA koordinator OUS og Tone Tønjum, professor og overlege UiO/OUS. Foto: Tahira Riaz tatt av Øystein Horgmo, foto Marta Gómez Muñoz tatt av Juan Gómez Muñoz, UiO, foto Pål Rongved tatt av Hampus Lundgren, forskning.no/UiO, foto Tone Tønjum tatt av Øystein Horgmo.

Tahira Riaz, postdoktor, UiO, Pål Rongved, professor, UiO, Marta Gómez-Muñoz, PhD student UiO / TTA koordinator OUS og Tone Tønjum, professor og overlege UiO/OUS. Foto: Tahira Riaz tatt av Øystein Horgmo, foto Marta Gómez Muñoz tatt av Juan Gómez Muñoz, UiO, foto Pål Rongved tatt av Hampus Lundgren, forskning.no/UiO, foto Tone Tønjum tatt av Øystein Horgmo.
Tuberkulose - TB
Postdoktor Tahira Riaz og PhD-student Marta Gómez-Muñoz forsker på ny terapi som har potensiale for å kunne brukes i behandlingen mot tuberkulose (TB), i Genomdynamikk (GD)-gruppen ledet av professor Tone Tønjum 1,2.
Målet er å oppdage nye medikamenter og deres virkningsmekanismer. Det tette samarbeidet mellom forskningsgruppen og klinikken i Avdeling for mikrobiologi og OUS for øvrig er av stor verdi. Det er også nært samarbeid mellom Pål Rongved, Farmasøytisk institutt, UiO 2,3 og Tønjum, Avdeling for mikrobiologi, UiO/OUS for å videreutvikle, teste og definere virkningsmekanismer for lovende nye forbindelser.
Nye komponenter utviklet i forskningsgruppen til Rongved viser hemming av bakterien Mycobacterium tuberculosis (MTB), årsaken til TB, i laboratoriet.
Økt forståelse av mekanismene som gir Mtb legemiddeltoleranse og antibiotikaresistens er viktig for å forbedre behandlingen og for å bidra til WHOs bærekraftsmål om å stoppe TB-epidemien innen 2030.
Tuberkulose spres ved luftsmitte. Illustrasjon: Colourbox.
Tuberkulose er et stort globalt problem
Verdens helseorganisasjon (WHO) har betydelig fokus på de to langsomme pandemiene tuberkulose (TB) og antimikrobiell resistens (AMR).
TB er en smittsom sykdom forårsaket av bakterien Mycobacterium tuberculosis (Mtb). Sykdommen påvirker oftest lungene og kan være dødelig hvis den ikke behandles. Ved lunge-TB sprer Mtb seg gjennom luften når mennesker med sykdommen hoster, nyser eller spytter.
Til tross for å være en helbredelig sykdom, dør mange i dag av TB. TB er den infeksjonen som årlig tar livet av høyest antall mennesker på verdensbasis (1.4 millioner dødsfall i 2019).
Årlig blir 10 millioner syke av TB. Imidlertid viser de fleste infiserte individer ingen sykdomssymptomer. Så mye som en fjerdedel av verdens befolkning antas å ha latent TB-sykdom (er smittet, men ikke syke).
TB-behandlingen må bli bedre
Behandlingen av TB er omfattende og langvarig, med mange bivirkninger. Normalt blir TB behandlet med kombinasjon av tre-fire antibiotika (isoniazid, rifampicin, pyrazinamid og evt etambutol) over en seks månedersperiode eller lenger, da Mtb er en langsomtvoksende bakterie.
Behandlingen er vanligvis effektiv, men det er viktig at den tas hele perioden for å forhindre tilbakefall og resistensutvikling. Ved påvisning av resistens mot noen av disse antibiotikaene, må behandlingen erstattes med andre medikamenter.
TB og antibiotikaresistens
I 2019 ble det påvist resistens mot isoniazid i 8% av tilfellene og rifampicin-resistens i 5% av tilfellene. Multi-resistent Mtb (resistens mot både isoniazid og rifampicin, MDR-TB) ble påvist hos om lag 465 000 mennesker med TB i 2019, og av disse var over 60 prosent ikke i stand til å få behandling. Blant MDR-TB har 6.2% extensively drug-resistant TB (XDR-TB; resistens mot de fleste antibiotika).
Antibiotikaresistens hos Mtb utvikles på grunn av genetiske mutasjoner i bestemte gener som har med antibiotikamålet å gjøre. For eksempel, gir punktmutasjoner i genet som koder for RNA polymerase B (rpoB) rifampicin-resistens.
Når det gjelder isoniazid, kan det være flere gener som er involvert i resistensutviklingen. Isoniazid er et «pro-drug», dette betyr at det trenger å bli aktivert for å virke. Hvis det blir mutasjoner i genet som koder for aktiveringsenzymet (katG), får vi bakterier som er resistente mot isoniazid. Idet isoniazid blir aktivert, dreper det bakterien ved å forhindre syntesen av mykolsyre, som er en unik og viktig komponent i celleveggen til Mtb. Oppstår det mutasjoner i genet som koder for enzymet involvert i dannelsen av mykolsyre (inhA), får vi også isoniazid-resistens.
Det er et økende problem med MDR-TB. Resistens kompliserer behandlingen betydelig; behandlingen er svært langvarig og dyr og har mange bi-virkninger. Det er fortsatt høy dødelighet ved multiresistent TB.
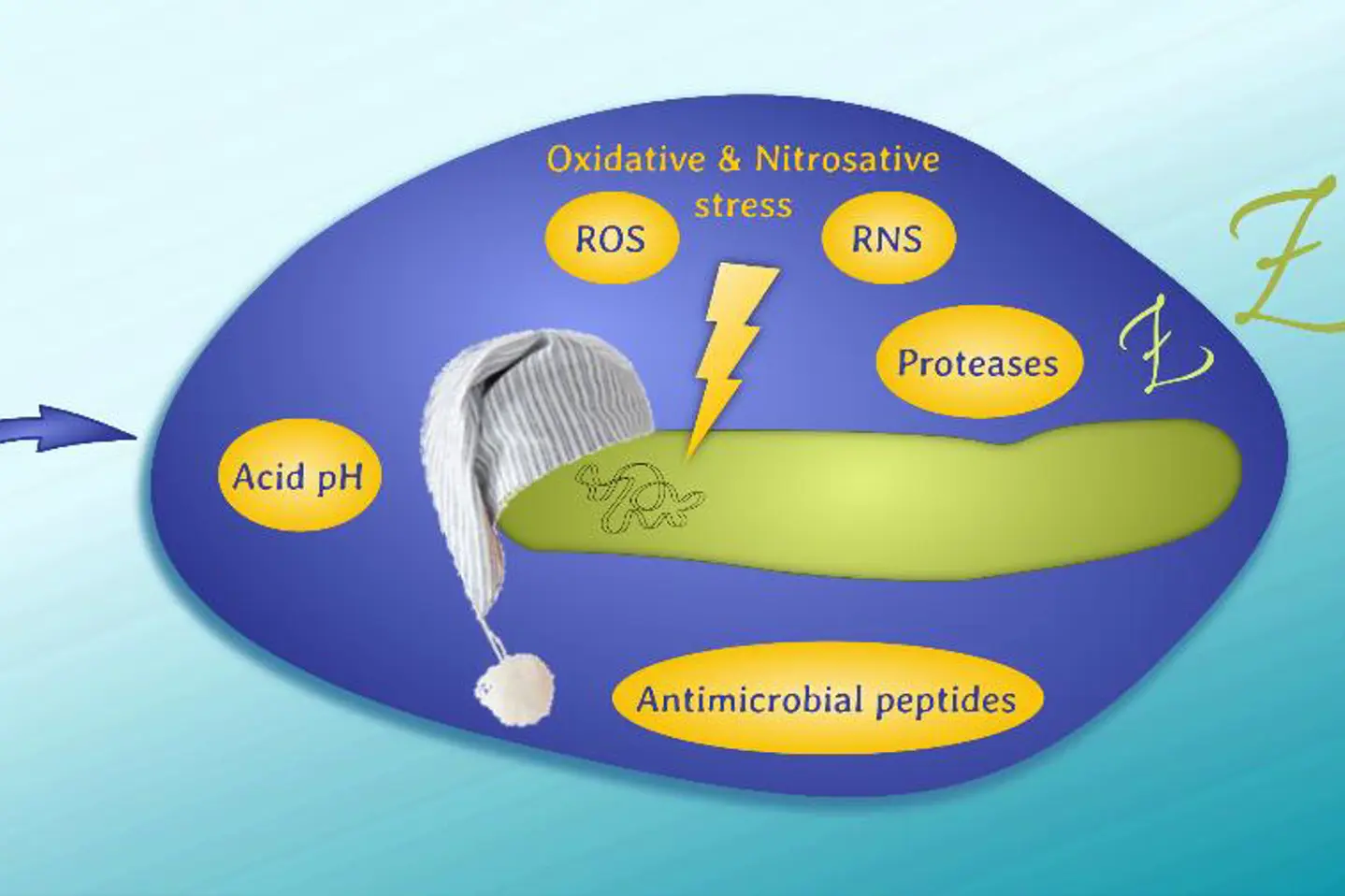
Tuberkulose (TB)-celler gjemmer seg i kroppen. De kan overleve og dele seg i det tøffe miljøet inne i kroppens makrofager. De kan også "gjemme" seg og legge seg til å "sove" i makrofager (latent TB), for så å våkne opp og dele seg igjen og gi sykdom (aktiv TB). Foto: Marta Gómez-Muñoz.
TB gjemmer seg i kroppen
I tillegg kan Mtb bli resistent mot antibiotika på en fenotypisk måte, uten å forandre sitt arvemateriale, gjennom å dorme eller «bli sovende» inne i kroppens makrofager. Mange antibiotika fungerer bare når Mtb-bakteriene deler seg (multipliseres), men når Mtb «sover», deler de seg ikke.
Dessuten klumper mykobakteriene seg sammen i hauger (biofilm), slik at de ikke blir tilgjengelige for behandlingen som gis. Mtb kan danne biofilm for å motstå stress-faktorene den møter på i kroppen. Biofilm-dannelse kan også motvirke antibiotika-effekten. Alt dette gjør at TB-behandling er en krevende utfordring.
COVID-19 og TB
I mange land har menneskelige, økonomiske og andre ressurser blitt omdisponert fra TB til COVID-19-responsen, mens datainnsamlings- og rapporteringssystemer også har blitt påvirket. Selv om økt smittevern under COVID-19-pandemien hemmer mange former for smitte inkludert TB, fremhever WHO at det var "betydelige reduksjoner" i rapporteringen og overvåking av nye tilfeller av TB i første halvdel av 2020, ettersom land innførte lock-down for å dempe spredningen av COVID-19. I tillegg har forstyrrelser i helsetjenester forårsaket av COVID-19-pandemien ført til ytterligere tilbakeslag, sier WHO.
Hvorfor frykter man flere TB-dødsfall når COVID-19-pandemien fortsetter? 'Betydelige reduksjoner' i helseinnsats for TB-pasienter er et utilsiktet resultat av lock-down på grunn av spredning av COVID-19. Det er derfor nødvendig med hastetiltak og finansiering for å opprettholde fremgang i den globale kampen mot TB, ifølge WHO. Midt i pandemien er det nå tid for å slå et slag for TB. Mens verdens land over hele verden sliter med COVID-19-pandemien, minner WHO om at TB fortsatt er verdens dødeligste smittsomme sykdom.
Mot slutten på tuberkulose: Stopp TB!
Mens anslagsvis 14 millioner mennesker ble behandlet for TB mellom 2018 og 2019, representerer de bare omtrent en tredjedel av de 40 millioner som WHO håper å behandle innen 2022. Ifølge WHO, selv om TB-tilfeller falt med 9 prosent og dødsfall med 14 prosent mellom 2015 og 2019, er tilgang til TB-tjenester fortsatt en utfordring rundt om i verden.
Sitat: "Rettferdig tilgang til kvalitet og rettidig diagnose, forebygging, behandling og pleie er fortsatt en utfordring", sier WHO-leder Tedros Adhanom Ghebreyesus i en pressemelding om TB-funnene i 2020.
"Det er presserende behov for akselerert handling over hele verden hvis vi skal nå våre mål innen 2022," oppfordrer han.
WHO har som mål å redusere TB med 40% innen 2022 og å utrydde sykdommen på verdensbasis innen 2030. Da må det nye medikamenter til.

Stort behov for nye medikamenter for å nå WHO's bærekraftsmål om å utrydde TB på verdensbasis. Foto: Colourbox.
Forskning på ny behandling
Vi undersøker nye forbindelser med stort potensiale for å kunne brukes som medikamenter i TB-behandling, sier Riaz. Vår samarbeidspartner Pål Rongved, leder av SYNFAS-gruppen ved Farmasøytisk instituttt UiO, har oppdaget en ny familie av fenazinderivater. Vi har vist at disse fenazinderivatene har stor aktivitet mot Mtb-isolater. Vi er i ferd med å utforske denne effekten videre også i andre bakteriearter.
Våre forskningspartnere i EU-samarbeidet JPI-AMR har utviklet en ny klasse med forbindelser, Mycobacterial Tolerance Inhibitors (MTIs), som har evnen til å hindre biofilm-dannelse i Mtb-laboratoriestammer 4,5. I tillegg viste disse forbindelsene evne til å re-sensitivisere isoniazid-resistente kliniske Mtb-stammer overfor isoniazid, når MTI ble brukt sammen med isoniazid.

Nye midler virker godt mot resistente tuberkulose-celler, her testet i REMA-assay. Foto: Håvard Homberset.
MTI virker godt mot ulike kliniske Mtb-isolater og vi er på spor av virkningsmekanismen, sier en godt fornøyd Riaz. Vårt nære samarbeid med klinikken gir oss en unik mulighet til å teste nye potensielle medikamenter i kliniske bakterie-isolater, og å oppdage virkningsmekanismene til disse forbindelsene i kliniske Mtb-stammer med ulik type og grad av resistens.
Forskning på kliniske Mtb-isolater gjør vi i vårt BSL3/P3-laboratorium, og virkningsmekanismene blir definert i detalj ved bruk av vårt høyteknologiske massespektrometri-utstyr. Massespektrometri er et kraftig verktøy i analyse av proteiner og hvordan de er dekorert (deres post-translasjonelle modifikasjoner, PTM). Analysen av proteiner og deres PTM utføres i sammenheng med cellenes komplekse funksjoner/nettverk ved hjelp av bioinformatikk og maskinlæring 6.
Samtidig analyserer Gómez-Muñoz hvordan Mtb-celler reagerer på stress på RNA-nivå. Hun har oppdaget Mtb-spesifikke små RNA-er som responderer på den formen for stress som finnes inne i makrofager og har nylig innlevert sin doktorgradsavhandling til UiO. Små RNAer kan i fremtiden også ha betydning i ny behandling mot TB. I tillegg studerer GD-gruppen effekten av et veksttilskudd som vekker opp «sovende» mykobakterier og derved forbedrer mykobakteriediagnostikk ved dyrkning. Denne mekanismen åpner også muligheter for ny TB-behandling.
- http://www.ous-research.no/tonjum/; https://www.med.uio.no/klinmed/english/research/groups/genome-dynamics/
- https://www.ttanetwork.net/
- https://www.mn.uio.no/farmasi/forskning/grupper/synfas/index.html
- https://www.umu.se/en/news/har-funnit-en-ny-strategi-att-behandla-tuberkulos_7890408/
- https://www.sciencedaily.com/releases/2019/06/190604094254.htm
- https://www.frontiersin.org/articles/10.3389/fmicb.2020.550760/full