Årsrapporter
Årsrapport NOSVAR 2022
Bakgrunn
Systemiske bindevevssykdommer og vaskulitter er sjeldne, men alvorlige autoimmune revmatiske sykdommer. De kjennetegnes ved revmatisk betennelse i bindevev som kan omfatte hud, ledd, indre organer og vevet omkring. Vaskulitt-sykdommer (vaskulitter) medfører betennelser i blodårer og organer.
De utløsende sykdomsårsakene er fortsatt ukjente, men når sykdommene først har startet, overreagerer immunsystemet med for stor aktivitet. Ved en feil angripes kroppens eget vev (autoimmunitet). De forskjellige sykdommene skilles ved at reaksjonen fra immunsystemet utløser ulike antistoff og skader forskjellige organer.
Blant bindevevssykdommene finner en systemisk lupus erytematosus (SLE), Sjøgrens syndrom, polymyositt, dermatomyositt, antisyntetase syndromet, systemisk sklerose og blandet bindevevssykdom (MCTD).
Vaskulittsykdommene består blant annet av temporalis arteritt, Takayasus arteritt, granulomatose med polyangiitt (GPA) (tidligere Wegeners granulomatose), Mikroskopisk polyangiitt (MPA), eosinofil granulomatose med polyangiitt (EGPA) (tidligere Churg Strauss syndrom), polyarteritis nodosa (PAN) og Behçets syndrom. Selv om mer detaljert kunnskap om immunsystemets funksjoner har gitt bedret forståelse av sykdomsmekanismene, mangler vi ennå effektiv behandling for flere av tilstandene. Systematisk inklusjon i registre legger grunnlag for forskning og resultater som bringer oss videre.
Historikk/Finansiering
Siden 1998 har Seksjon for revmatologi ved OUS, Rikshospitalet og tidligere Oslo Sanitetsforening Revmatismesykehus bygget opp et stort, samtykkebasert forsknings- og kvalitetssikringsregister for systemiske bindevevssykdommer og vaskulitt (Norsk systemisk bindevevssykdom og vaskulittregister, NOSVAR). RHI biobank (revmatologi, hud og infeksjon) og et samtykkeregister er knyttet til NOSVAR. Registeret er utelukkende finansiert gjennom offentlige midler via Seksjon for revmatologi, OUS, Rikshospitalet og har dermed ingen relasjoner til farmasøytisk industri eller andre kommersielle aktører. Midlene går til en stilling for registerkoordinator/rådgiver (siden 2000), en deltidsansatt overlege (siden 2008) og IT- og driftskostnader (siden 1999). NOSVAR er blitt det største registeret i sitt slag i landet med snart 4700 inkluderte pasienter.
Administrativt og faglig ansvar
Oslo Universitetssykehus (OUS) er eier og behandlingsansvarlig for NOSVAR. Seksjon for Revmatologi ved overlege dr. med Øyvind Palm administrerer registeret. Overlegen rapporterer direkte til seksjonsleder og utarbeider årsrapport i samarbeid med registerkoordinator Torhild Garen. Registerkoordinatoren står for den daglige drift av registeret og utarbeider rapporter til styret i RHI biobanken.
Juridisk hjemmelsgrunnlag
- Heleseregisterloven, jan 2015
- Lov om medisinsk og helsefaglig forskning (helseforskningsloven)
- Konsesjon Datatilsynet til 2028
Bredt samtykke og hva det dekker
- Bruk av journaldata
- Kobling til Biobanker
- Behandlingsrettede helseregistre
- Kobling til samtykkeregister
- Kobling Kreftregisteret
- Medisinsk fødselsregister
- Dødsårsaksregsiteret
- Nasjonalt pasientregister
- Reseptregister
- Opplysning fra fastlege
- Opplysning fra andre helseforetak m flere
- Alle typer studier og kvalitetssikring
Informasjonsplikt
Deltakerne får muntlig og skriftlig informasjon og kan følge via NOSVARs internettside informasjon om hvilke formål personopplysningene og/eller humant biologisk materiale benyttes til.
Styingsgruppen/Referansegruppen
Styringsgruppen består av:
- professor dr. med Øyvind Molberg
- overlege PhD Ragnar Gunnarsson
- overlege dr. med Øyvind Palm
- overlege Øyvind Midtvedt
- registerkoordinator Torhild Garen
Referansegruppen:
- seksjonsleder ved seksjon for revmatologi, OUS, Rikshospitalet
- avdelingsoverlegene ved eksterne avdelinger som eventuelt deltar i registreringene. Større endringer i registeret diskuteres i styringsgruppen før vedtak fattes.
Registrering og data
Alle pasienter over 18 år som har/har fått en sikker systemisk bindevevssykdom eller vaskulitt vil bli forespurt om deltakelse i NOSVAR. En forutsetning er at diagnosen er sikker og at pasientene er samtykkekompetente.
- Registrering i NOSVAR registeret blir gjort i forbindelse med konsultasjoner ved poliklinikken, dagenheten eller sengeposten ved Seksjon for revmatologi, Oslo Universitetssykehus. Eksterne pasienter inkludert i samarbeidsstudier kan bli forespurt av eksterne leger (andre sykehus rekrutterer til oss) om deltakelse i NOSVAR. Tilpasset samtykkeskriv til dette formål er godkjent av REK. De fleste registreringer baseres på data fra sykejournalen. Registreringen tar vanligvis få minutter å gjennomføre og gjøres samtidig med rutinekonsultasjoner.
- De mest sentrale data omfatter diagnose, tidspunkt for sykdomsdebut, diagnoseår, symptomer og manifestasjoner i henhold til klassifikasjonskriterier og karakteristiske antistoff. Pasientene registreres som regel en gang, med unntak av diagnosen systemisk sklerose som har oppfølgingsregistreringer.
- Som en del av registreringen spør vi pasientene også om lov til å ta blodprøver for forskning. Prøvene oppbevares i biobank for revmatologi, hud- og infeksjonssykdommer (RHI-biobank).
Nytt i 2022 Sammedrag
Først og fremst vil vi rette en stor takk til alle pasienter som har samtykket til deltagelse i NOSVAR i 2022. Takk også til ledere, leger og sykepleiere som bidrar til registrering og ser nytteverdien i dette arbeidet.
Dette er den 22. årsrapporten som er utgitt av NOSVAR registeret. Vi håper at årsrapporten er interessant, og at den kan brukes til motivasjon for forskning - og kvalitetsarbeid fremover.
Målsettingen om et høyt antall nye pasienter til registeret er også nådd i 2022. Et betydelig antall SLE pasienter inkluderte fra eksterne sykehus har bidradd til økningen.
- 4702 pasienter inkludert siden oppstarten av registeret i 1999
- 31 publikasjoner i 2022. 163 totalt mellom 2010 og 2022 med data fra register og RHI-biobank
- Tilsammen 13 abstracts i 2022 er presentert på EULAR (Europeisk revmatologi kongress, København) og ACR (American congress of rheumatology, Philadelphia, USA)
NOSVAR brukes stadig i nye, prosjekter. Et eksempel er NOR-SLE kohorten, et samarbeid på tvers av alle revmatologiske avdelinger i hele Helse Sør-Øst (HSØ). Rundt 1600 personer med Lupus i HSØ i perioden 1999-2017 er inkludert i studien. Med det er Nor-SLE kohorten en av de største befolkningsbaserte Lupus kohorter på verdensbasis og utmerker seg med lang oppfølgingstid. Eksterne pasienter inkludert i studien har gitt sitt samtykke til inklusjon i NOSVAR og dermed bidradd til økt antall registrerte i 2022.
En annen pågående studie er NOR IgG4 studien. På samme måte som ved NOR-SLE har pasienter som ikke er inkludert i NOSVAR fått tilsendt informasjonsskriv om studien og NOSVAR-samtykke. Innsamlede data vil på sikt bli importert til NOSVAR til bruk i eventuelle oppfølgingsstudier.
I desember ble den planlagte utvidelsen av registeret med inntrekk av lab-data ferdigstilt, et samarbeid som startet i 2021 med Klinisk datavarehus (KDVH) og Medinsight. En egen «lab-ark»-fane er tilgjengelig hvor man kan trekke inn lab-prøver fra 2004 til dagens dato. Funksjonen vil gi økt nytteverdi av NOSVAR ved at labsvar knyttet til pasientenes inklusjonsdato vil være lett tilgjengelig.
Skanning av over 3.300 historiske samtykker til samtykkeregisteret (1999-2018) ble avsluttet høsten 2022.
Det jobbes med muligheten for å samtykke elektronisk for så å overføre disse til samtykkeregisteret. Endelig ferdigstillelse ventes primo 2023.
Målsettingen om å supplere med prøvetaking av NOSVAR- pasienter som mangler blodprøver ble dessverre ikke nådd i 2022. Vi så også en klar nedgang i antall nye donorer og prøvetaking av serielle prøver. En vesentlig årsak er at prøvetakningen av økonomiske grunner og stramt avdelingsbudsjett måtte stanses fra aug/sept 2022 ved kvote på 190 prøver. Dette er en uheldig utvikling som på sikt kan få konsekvenser for målsettingen om mange fremtidige publikasjoner og utvidet samarbeid med andre forskere nasjonalt og internasjonalt.
Generelt
Over 4700 pasienter er inkludert i NOSVAR siden inklusjonene begynte i 1999, fordelt på 46 ulike bindevev- og vaskulitt diagnoser.
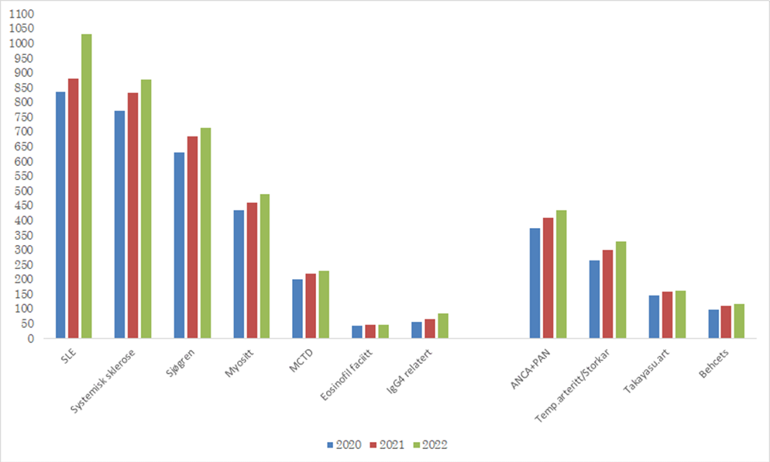
I 2022 ble det inkludert 388 nye pasienter i NOSVAR, en økning på 16 % sammenlignet med året før. Oppgangen skyldes i hovedsak økt inkludering av 137 eksterne SLE pasienter. Figur 1 viser SLE som den største diagnosegruppen i registeret med totalt 1031 pasienter. Flest nye registreringer sammenlignet med året før ble gjort på SLE og IgG4.
Oversikt over antall pasienter per diagnose er vist i Tabell 1a og 1b. Totalt 54 pasienter er registrert med mer enn en primær diagnose. De største diagnosegruppene innen bindevevssykdommer og vaskulitter er vist i Figur 1.
Systemisk sklerose er et satsningsområde. I registreringene inngår trepasientrapporterte skjemaer; SF36, SHAQ og UCLA-GIT skår. Disse måler henholdsvis livskvalitet, funksjon i dagliglivets aktiviteter og symptomer relatert til mage og tarm. De fleste oppfølgingsregistreringene gjøres ved konsultasjoner for systemisk sklerose-poliklinikken.
| Bindevevssykdommer | 2022 | Total | |
| C96.1 | Erdheim-Chester | 3 | |
| D68.8 | Antifosfolipidsyndrom | 1 | 40 |
| D86.8 | Sarkoidose | 6 | 36 |
| D69.0 | Henoch-Schönlein purpura | 2 | 13 |
| D46.7 | VEXAS | 4 | 11 |
| E85.0 | Familiær Middelhavsfeber(FMF) | 3 | |
| J84.8 | IPAF (interstitiell pneumoni med autoimmune kjennetegn) | 4 | |
| K66.2 | Retroperitoneal fibrose (ikke IgG4 relatert) | 1 | 5 |
| L50.2 | Schnitzler syndrom | 2 | |
| M06.1 | Adult Stills sykdom | 3 | 26 |
| M32.0 | Legemiddelutløst systemisk lupus erythematosus | 8 | |
| M32.1 | Systemisk lupus erythematosus med aff av nærmere bestemt organ | 4 | 196 |
| M32.8 | Andre spesifiserte former for systemisk lupus erythematosus | 3 | 143 |
| M32.9 | Uspesifisert systemisk lupus erythematosus | 146 | 687 |
| M33.0 | Juvenil dermatomyositt | 1 | 30 |
| M33.1 | Annen dermatomyositt | 9 | 88 |
| M33.2 | Polymyositt | 4 | 99 |
| M60.8 | Inklusjonslegememyositt | 5 | 75 |
| M33.9 | Uspesifisert dermatomyositt | 1 | 17 |
| M35.8 | Antisyntetase syndrom | 9 | 181 |
| M34.0 | Progressiv systemisk sklerose (diffus form) | 7 | 201 |
| M34.1 | CREST-syndrom | 25 | 616 |
| M34.8 | Andre spesifiserte former for systemisk | 12 | 51 |
| M34.9 | Uspesifisert systemisk sklerose | 1 | 9 |
| M35.0 | Sjøgrens syndrom | 30 | 715 |
| M35.1 | MCTD | 8 | 228 |
| M35.4 | Diffus eosinofil fasciitt | 2 | 47 |
| M35.5 | Multifokal fibrosklerose (IgG4) | 13 | 83 |
| M35.6 | Weber-Christian pannikulitt | 3 | |
| M94.1 | Relapsing Polychondritis | 4 | 29 |
| M05.1 + J99.0 | Revmatoid lungesykdom | 22 | 54 |
| Totalt | 323 | 3703 |
| Vaskulitter | 2022 | Total | |
| M30.0 | Polyarteritis nodosa (PAN) | 4 | 39 |
| M30.1 | Churg-Strauss' sykdom (EGPA) | 8 | 67 |
| M31.3 | Wegeners granulomatose (GPA) | 11 | 265 |
| M31.4 | Aortabuesyndrom (Takayasus arteritt) | 3 | 160 |
| M31.5 | Kjempecellearteritt med polymyalgia revmatika | 6 | 133 |
| M31.6 | Annen kjempecellearteritt | 24 | 198 |
| M31.7 | Mikroskopisk polyangiitt (MPA) | 4 | 65 |
| M31.8 | Cogan’s syndrom | 6 | |
| M31.9 | Uspes. vaskulitt periaortitt mm | 2 | |
| M35.2 | Behcets | 5 | 116 |
| I67.7 | Cerebral vaskulitt | 5 | |
| Totalt | 65 | 1056 |
| 2022 | Totalt | ||
| Bindevevssykdommer | 323 | 3703 | |
| Vaskulitter | 65 | 1056 | |
| Totalt | 388 | 4759* |
*50 pasienter er registrert med flere enn en primærdiagnose.
Figur 1: Figuren viser det årlig økende antall pasienter for et utvalg diagnoser i NOSVAR. Bindevevssykdommer (venstre side) og vaskulitter (høyre side), året 2020, 2021og 2022 er illustrert med henholdsvis lys blå, rød og grønn farge.
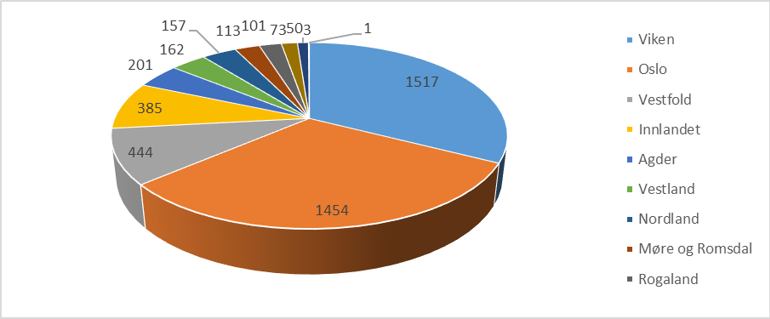
Figur 2: Fylkesvis fordeling av inkluderte pasienter i NOSVAR 2022
Mortalitet og alder ved død
I perioden 1999 -31.12.2022 er 879 av de inkluderte pasientene døde (mors) (18 %), herav døde 83 i 2022. Median alder IQR (25th, 75th) ved død for kvinner var 74 år (63, 81) og menn 71 år (64, 79) som er lavere enn forventet i befolkningen, (kvinner 85 år og 82 år for menn). Disse pasientenes median alder IQR (25th, 75th) var ved sykdomsdebut 56 år (42, 67), diagnosetidspunkt 60 år (47,69) og inklusjon 65 år (55, 73).
RHI-biobanken
Forskningsbiobank for Avdeling for Revmatologi, Hud- og Infeksjonssykdommer (RHI-Biobanken), organisering og styring er omtalt i årsrapporten 2018.
RHI-biobank benytter e-Biobank som system for sporing av prøvemateriale. Dessverre er det komplisert å koble data i RHI-biobank med kliniske data i NOSVAR/Medinsight for generering av rapporter. Høsten 2022 har RHI biobanken fått tilknyttet en 30 % fast bioingeniør lønnet av driftsmidler fra OUS.
Aktiviteten i 2022
Totalt ble 288 prøver er avsatt til RHI biobanken i 2022, en reduksjon på 57 % sammenlignet med året før (504). På grunn av kostnader for prøvetakning og prosessering og strammere avdelingsbudsjett, ble det i fastsatt en årlig kvote på 300 prøver fordelt på Revma- (190), hud-(40) og infeksjonsseksjonene (70). For revma-seksjonen gikk begrensingen særlig ut over prøvetaking av serielle prøver og påfyll av oppbrukt materiale for forskning på systemisk sklerose- som har vært et satsningsområde i mange år. Nye NOSVAR-pasienter ble prioritert, men mange kunne likevel ikke avlegge prøvemateriale til biobanken. For å sikre flest mulig prøver fra nye inneliggende eller dagpasienter, ble en ny prosedyre avtalt. Blodprøvetaking ble ihht denne utfør av sykepleiere ved dagenheten/sengeposten, kun nye pasienter ble prioritert, og bare serum og fullblod ble prosessert. Dette forutsatte tilstrekkelige sykepleierresurser og daglig avtale med bioingeniøren som måtte være tilgjengelig for prosessering av prøven. Løsningen fungerte ikke alltid optimalt, siden både sykepleierne og bioingeniøren primært også har andre oppgaver. Dette forklarer at kun 38 prøver ble avsatt høsten 2022. Vi skylder uansett ledende seksjonssykepleier Anders Engebråten, alle involverte sykepleiere og bioingeniørene en stor takk for ekstraordinær innsats!
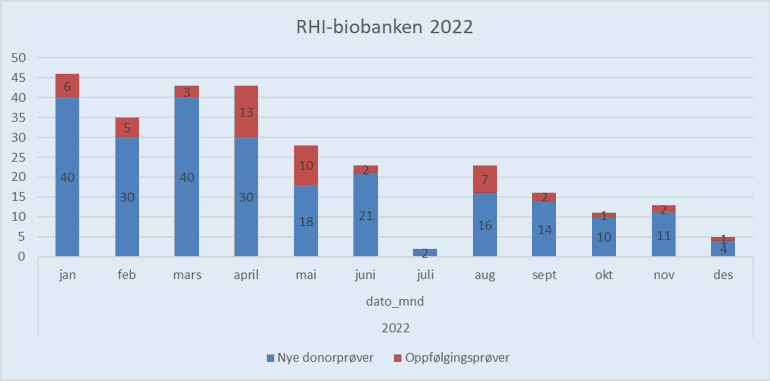
Figur 3a: Antall nye donorprøver (blå farge) og oppfølgingsprøver (rød farge) avsatt til RHI-biobanken 2022.
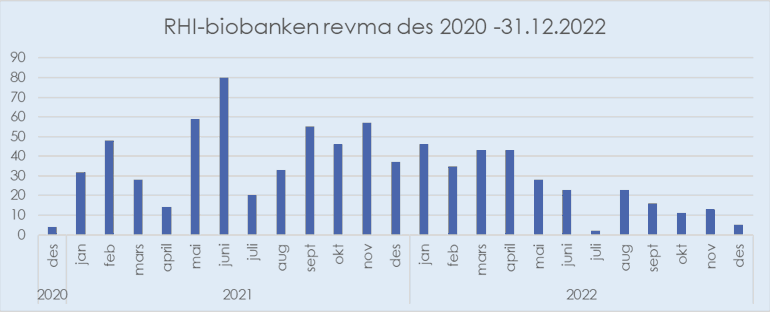
Figur 3b: Antall donorprøver avsatt til RHI-biobanken siden oppstarten av RHI biobanken i des 2020 –des 2022
Rutiner for registrering /registreringsverktøy
Rutiner for registrering
Gode rutiner for registrering og rekvirering av blodprøver til RHI biobanken er nødvendig for å få inkludert pasienter i register og biobank.
Vår faste medarbeider på sengeposten gjennom mange år, Kari Fresjar, sluttet i jobben i 2022. Vi takker Kari for innsatsen, for det solide arbeidet hun gjorde for å inkludere pasienter til registeret og for å påminne legene om registreringene. Inklusjoner på sengeposten er i ettertid forsøkt løst ved at nye pasienter får en merknad i innleggelseslisten at pasienten ønskes registrert i NOSVAR. Pasienter som ikke ble registrert ved diagnosetidspunktet, skal fanges opp av registerkoordinator ved neste kontroll. Sekretæren på sengeposten leverer samtykkeskjema og blodprøverekvisisjonen til sykepleier som har ansvaret for pasienten. Sykepleier og ved behov også lege informerer om hva samtykket innebærer (informert bredt samtykke). Også i 2022 har samarbeidet med Revma-sykepleierne og sekretærer på Dagenheten, sengeposten og poliklinikken vært uvurderlig mht den daglige driften av registeret.
Utvidet registrering på SSc - status i 2022
Utvidet registrering for forskning på satsingsområdet systemisk sklerose har vært ønsket lenge. Planleggingen av arbeidet startet opp i 2020.
Hensikten er å legge til/endre variabler i NOSVAR for å kunne eksportere data til det Europeiske Systemisk sklerose registeret (EUSTAR). En kartlegging av fellesvariabler i NOSVAR og EUSTAR er gjort. Målet var å overføre data elektronisk fra NOSVAR til EUSTAR i løpet av 2021. På grunn av stort arbeidspress og covid-19 ble dette arbeidet lagt litt på vent. Videre er det planlagt en ny funksjon der variabler fra NOSVAR genererer en rapport / utkast til journalnotat i pasientenes journal i DIPS. Planlegging videreføres til 2023. For systemisk sklerose ønsker vi også import og oppbevaring av mer komplette, samtykkebaserte data innhentet i forskningsprosjekter. Dette er i utgangspunktet pasienter fra registeret der et betydelig arbeid er gjort for å sikre kompletthet og validiteten av data. Av økonomiske årsaker ble ikke dette arbeidet ferdig i 2022, og videreføres til 2023.
Registrering av PROMS
Systemisk sklerose-pasienter har ved inklusjon, de første 5 årene etter diagnose og deretter annet hvert år, fylt ut SF36 HAQ, UCLA Git skår (måler henholdsvis pasientenes livskvalitet, funksjon og mage/tarm plager). Skjemaene er papirbasert og har vært skannet til Access database ved hjelp av Teleform. Skanning av skjema har dessverre ikke vært mulig å gjennomføre etter oppgradering til Windows 10 på OUS. Dette skyldes gammel versjonen av Teleform som ikke fungerer mot Access 16. Sykehusparter gjennomfører en kartlegging av brukere av Teleform Forskning for å undersøke behovet for denne tjenesten fremover. Det er ennå ikke avklart om sykehuset vil prioritere denne tjenesten. Vi avventer tilbakemelding fra Sykehuspartner med en eventuell alternativ løsning. Inntil en avklaring foreligger blir ikke PROMS data registrert til databasen.
Pågående og nye prosjekter
SLE
Nor-SLE
Prosjektansvarlig: MD PhD Karoline Lerang
Stipendiat: Hilde Haukeland, overlege ved revmatologisk avdeling Martina Hansens Hospital
Veileder; MD PhD Karoline Lerang, prof. dr. med. Øyvind Molberg
Stipendiat: lege Sigrid Reppe Moe, Oslo Universitetssykehus.
Veileder; Karoline Lerang, dr. med Sella Provan og prof. dr. med. Øyvind Molberg.
REK sør-øst: 2009/2577.
Nor-SLE er et samarbeidsprosjekt på tvers av alle revmatologiske avdelinger i hele Helse Sør-Øst (HSØ) som utgår fra Revmatologisk forskningsgruppe ved Oslo Universitetssykehus, Rikshospitalet. Målet er å øke kunnskapen om forekomst av og sykdomsforløp ved Systemisk Lupus Erytematosus (Lupus) Arbeidet med etableringen av kohorten ble ledet av Dr. (PhD) Karoline Lerang og Professor Øyvind Molberg. PhD kandidat og revmatolog Hilde Haukeland ser på insidens og prevalens av SLE i HSØ, klassifikasjonskriterier, fenotyper og kreftforekomst. PhD kandidat og lege Sigrid Reppe Moe undersøker faktorer ved Lupus som kan påvirke prognose og forhindre utvikling av sykdomskomplikasjoner.
Prosjektet har funnet rundt 1600 personer med Lupus i HSØ i perioden 1999-2017. Med det er Nor-SLE kohorten er en av de største befolkningsbaserte Lupus kohort på verdensbasis og utmerker seg med lang oppfølgingstid.
Etableringen av kohorten var omfattende, og mere krevende enn det noen av oss hadde forestilt oss da vi startet, men nå gleder vi oss stort over at databasen endelig er på plass, slik at vi kan gjøre god vitenskap og lære mye mer.
Kohorten vil gi et godt utgangspunkt for klinisk viktig forskning i flere år fremover. For å få lov til å følge kohorten videre er vi i ferd med å samle inn samtykker til NOSVAR. Dette store arbeidet hadde ikke vært mulig å gjennomføre uten godt samarbeid innen regionen (revmatologisk avdeling ved Sykehuset Østfold, Vestre Viken og Sørlandet Sykehus, Revmatismesykehuset Lillehammer, Martina Hansens Hospital, Betanien Hospital, samt nyreavdeling ved Akershus Universitetssykehus og Sykehuset i Vestfold og privatpraktiserende revmatologer i helse Sør-Øst ), og økonomisk støtte fra Norske Kvinners Sanitetsforening (N.K.S.), stiftelsen DAM, Vivi Irene Hansens fond, Ragna og Eigil Eikens legat for revmatismeforskning og Norsk revmatikerforbund (NRF).
Systemisk sklerose
Systemisk sklerose/Biomarkørstudie
Prosjektansvarlig: prof. dr. med. Øyvind Molberg, ved seksjon for revmatologi.
Stipendiat: Henriette Didriksen, master i molekylærbiologi, stipendiat fra sept. 2016
REK sør-øst: REK sør-øst: 2018/674 Utfalls relaterte biomarkører ved systemisk inflammatorisk Revmatiske sykdommer.
Prosjektet utføres som en biomarkør studie med materiale fra systemisk sklerose-pasienter og friske kontroller. Prosjektet omhandler sammenhengen mellom sykdom og nivå av potensielle lymfatiske biomarkører i serumprøver, og deres lokalisering i vev fra pasienter med systemisk sklerose. Arbeidet består av tre arbeidsplaner: 1) Analysere nivået av de lymfatiske faktorene VEGF-C, VEGFR3, Ang-2 og Tie-2 i systemisk sklerose pasienter. 2) Karakterisering av CCL21 på molekylært nivå hos systemisk sklerose pasienter og lokalisering av CCL21 i lungevev fra systemisk sklerose pasienter som har utviklet pulmonal arteriell hypertensjon. 3) Analysere duodenale biopsier fra systemisk sklerose pasienter før og etter fekal mikrobiota transplantasjon (ReSScue pilot), sammenlignet med duodenale biopsier fra systemisk sklerose kontrollgruppe og friske kontroller. Serumprøver og biopsier som inngår i prosjektet er en del av NOSVAR. Tredje artikkel forventes publisert primo 2023.
Systemisk sklerose/Lungefibrose
Prosjekt tittel: “Identification of novel tools for cardiopulmonary risk prediction in systemic sclerosis”.
Prosjektansvarlig: senioforsker Anna-Maria Hoffmann-Vold
Stipendiat: lege Imon Barua
REK sør-øst: REK (2016/11).
Systemisk sklerose/Pulmonal hypertensjon (PAH)
Prosjektansvarlig: MD PhD Anna-Maria Hoffmann-Vold Seksjon for revmatologi.
Stipendiat: lege Hilde Bjørkekjær.
REK sør-øst: Utarbeides
Flere studier og data fra den komplette, nasjonale SSc-kohorten tyder på at PAH ikke oppdages tidlig nok og er avhengig av pasientenes bosted. Dette prosjektet vil belyse to viktige spørsmål: 1. Hvordan kan vi påvise PAH tidlig nok? 2. Hvordan kan vi få til likeverdig utredning, diagnostikk og oppfølging av PAH for alle norske pasienter?
Ig coating av tarmbakterier ved tidlig SSc
Prosjektansvarlig: MD PhD Anna-Maria Hoffmann-Vold
Samarbeidspartner: post. doc Brian Chung (Norsk senter for PSC), Kristofer Andreasson og Roger Hesselstrand, Revmatologisk avdeling, Skåne Universitetssykehus
REK sør-øst: 2014/2330 Tarmens bakterieflora ved systemisk sklerose
Abstract presentert på EULAR 2020. Artikkel skrives
ReSScue studien: Transplantasjon av tarmbakterier ved Systemisk sklerose
Prosjektleder: prof. dr. med. Øyvind Molberg, Anna-Maria Hoffmann-Vold (postdoc).
REK helse-sør: 2016/1529 Standardisert fekal mikrobiota transplantasjon ved systemisk sklerose
Nasjonal samarbeids-studie: Oslo universitets sykehus, St. Olavs hospital, Trondheim, Universitetssykehuset Nord-Norge, Tromsø, Haukeland universitetssykehus, Bergen, Karolinska institutet.
En internasjonal ekspertgruppe på systemisk sklerose er etablert i forbindelse med studien: Oliver Distler (Zurich, Switzerland), Dinesh Khanna (Michigan, USA) og Elizabeth Volkmann (UCLA, USA). 77 pasienter fra NOSVAR er screenet, 60 er inkludert. Studien ble avsluttet i juni 2022. Offentliggjøring av resultater, diskusjon og planlegging av publikasjoner i forbindelse med studien ble avholdt på Scandic Hotel, Holmenkollen 4.nov 2022.
Insidens av renal krise ved SSc
Prosjektansvarlig: Scleroderma Clinical Trials Consortium (SCTC), USA, multicenter studie
Prosjektmedarbeider: MD PhD Anna-Maria Hoffmann-Vold
Rek sør øst: REK (2016/119). NOSVAR
SRC (scleroderma renal crisis) er en arbeidsgruppe under SCTC som ble dannet i 2015 og består av internasjonale eksperter innen revmatologi, nevrologi og patologi. Gruppen jobber med utvikling og validering av klassifikasjonskriterier av renal krise (SRC). Hensikten med samarbeidet er å måle insidensen av renal krise i en større populasjon. Studien er avsluttet. Artikkel under bearbeiding.
Langtids sikkerhet studie av Nintedanib i sklerodermi
Prosjektansvarlig: Boehringer Ingelheim
Norsk koordinator utprøver: MD PhD Anna-Maria Hoffmann-Vold
Rek sør øst: 2018/1332
Senscis-On studien som ble startet i 2018 når Senscis ble avsluttet for å analysere langtidseffekt av Nintedanob på SSc-ILD.
OUS har inkludert 3 pasienter fra NOSVAR.
Interstitiell lungesykdom ved SSc og IPF
Prosjektansvarlig: MD PhD Anna-Maria Hoffmann-Vold
Prosjektmedarbeider: MD Michael Kreuter, lungelege Thoraxklinik Heidelberg, Tyskland, MD PhD Håvard Fretheim, MD Phuong Phuong Diep, lungeavdelingen RH, OUS
Rek sør øst: #187504
Longitudinell observasjonsstudie. Alle pasienter med SSc-ILD fra NOSVAR og IPF pasienter fra tyske INSIGHTS registeret skal analyseres mtp sykdomsprogresjon, behandling, behandlingseffekt og utfallsmål.
OUS inkluderer ca 300 pasienter med SSc-ILD fra NOSVAR. I tillegg inkluderes det ca 1000 IPF pasienter fra INSIGHTS. Artikkel skrives.
Hjemmespirometri ved progressiv interstitiell lunge sykdom
Prosjektansvarlig: MD PhD Marlies Wijsenbeek, Erasmus University, Rotterdam, Nederland
Prosjektmedarbeider: MD PhD Anna-Maria Hoffmann-Vold, MD Mike Durheim, lungeavdeling, RH, OUS
Rek sør øst: #145905
Alle pasienter med ny diagnostisert og progressiv ILD skal inkluderes i et internasjonalt register og følges opp med hjemme spirometri hvor data samles inn via en app og lagres på en sikker server i Nederland.
OUS har inkludert 3 pasienter fra NOSVAR så langt.
ILD risk score in SSc
Prosjektansvarlig: MD Cosimo Bruni University Hospital of Zurich, Sveits
Prosjektmedarbeider: MD PhD Anna-Maria Hoffmann-Vold, MD PhD Håvard Fretheim
REK sør-øst: 2017/1816 Interstitiell lungesykdom ved SSc
Dette er en multisenter studie fra 5 land (Sveits, Norge, Nederland, Italia, Tyskland) for å identifisere en risiko score for utvikling av ILD. Kliniske data fra SSc pasienter i NOSVAR er inkludert i studien. Artikkel under skriving.
Interstitiell lungesykdom ved bindevevssykdommer og leddgikt
Prosjektansvarlig: MD PhD Anna-Maria Hoffmann-Vold
Prosjektmedarbeider: MD Phuong Phuon Diep, lungeavdelingen RH, OUS, MD PhD Trond Mogens Aaløkken, radiologisk avd, RH, OUS, MD John Belperio (lungeavdeling), Grace Kim og Jonathan Goldin (radiologisk avdeling) UCLA (University of California), Los Angeles, USA
Rek sør øst: #187572 REK har også gitt dispensasjon fra regelen om å innhente aktivt samtykke for avdøde pårørende med revmatisk sykdom (bindevevssykdommer og leddgikt).
Longitudinell observasjonsstudie. Alle pasienter med bindevevs sykdommer og RA med ILD blir tilsett av revmatolog og lungelege, kartlagt med lunge funksjon og HRCT, pasient rapporterte utfallsmål (PROMs)prøver til NOSVAR og dyp neseprøve til analyse på UCLA ved baseline og 12 måneder. Alle pasienter blir registrert i NOSVAR.
Det planlegges å inkludere 150 CTD-ILD pasienter fra NOSVAR. Ferdig med 130 pasienter baseline.
ILD quantification on serial HRCT
Prosjektansvarlig: MD PhD Anna Maria Hoffmann Vold
Prosjektmedarbeider: Grace Kim, Jonathan Goldin, UCLA USA
Rek: 187572
Serielle HRCT fra 500 pasienter fra NOSVAR ble sendt til UCLA. Kvantifisering av lungefibrose er avsluttet. Resultater må tolkes og publiseres.
RA-ILD patient survey
Prosjektansvarlig: MD PhD Anna Maria Hoffmann-Vold og Michael Kreuter, Thoraxklinik Heidelberg, Tyskland
REK: Heidelberg
Spørreskjema til RA pasienter med og uten lungefibrose. 250 norske pasienter har svart, derav ca 40 NOSVAR RA-ILD pasienter. Abstract sendt til EULAR og ERS 2023, Artikkel under utarbeiding.
Biomarker analysis for ILD progression in systemic sclerosis
Prosjektansvarlig: MD PhD Anna Maria Hoffmann Vold
REK: 2016-119 NOSVAR
Multicenter biomarkør studie (ca 1000 pasienter, derav ca 200 NOSVAR prøver), i tillegg Zurich, Paris, Erlangen og Praha har sendt prøver Analysene kjøres av Thor Ueland, venter på resultater.
Molecular profiling of nasal swabs in CTD-IL
Prosjektansvarlig: MD PhD Anna Maria Hoffmann Vold
REK:187572
Medarbeider: John Belperio, UCLA, USA, Oliver Distler, Universitets sukkehus Sveits
Neseprøver fra NOSVAR CTD-ID pasienter sendes til UCLA til RNA analyser.
Vaskulitter
Behçets sykdom i Norge
Tittel: En kartlegging av pasienter i Oslo
Prosjektleder: lege Jin Lisa Lorentsen
Prosjektmedarbeider: dr. med. Øyvind Palm og MD PhD Karoline Lerang (postdoc).
REK sør-øst: godkjent feb 2022, ref nr 382756
Behçets sykdom er en kronisk blodårebetennelse som oftest rammer unge personer. Sykdommen debuterer hyppigst med tilbakevendende munn- og genitale sår, men en rekke andre organer kan også angripes. Diagnosen baseres hovedsakelig på klinisk vurdering av symptomer og undersøkelsesfunn, der forskjellige spesialister er involvert. Studier fra andre land har vist en diagnostisk forsinkelse fra symptomstart til diagnose på gjennomsnittlig 8 år. Milde variant av sykdommen forekommer, slik at noen pasienter sannsynligvis aldri blir diagnostisert. Behçets sykdom er ikke tidligere studert nærmere i Norge.
I dette prosjektet ønsker vi å skaffe informasjon om Behçets sykdom i Norge. Vi ønsker å gjøre en retrospektiv gjennomgang av pasientjournaler i OUS i tillegg til å bruke data fra forskningsregisteret NOSVAR som har samlet informasjon over en tidsperiode på 23 år. Hovedhensikten er å skaffe epidemiologisk informasjon om Behçets sykdom i Norge, kartlegge sykdomsmanifestasjoner, bidra til raskere diagnostisk avklaring, bedret pasientflyt og tidlig igangsetting av riktig behandling for pasientene i fremtiden.
IgG4-RELATERT SYKDOM (Nor_IgG4 studien)
Prosjekt tittel: Identifisering av pasienter med IgG4-RD.
Prosjektansvarlig: På OUS: MD PhD Anna-Maria Hoffmann-Vold.
Stipendiat: lege Jens Vikse.
REK sør-øst: Under utarbeidelse
Prosjektet vil bestå av to deler:
Del 1: Retrospektiv gjennomgang av pasientjournalen av alle pasienter fra NOSVAR
Del 2: Én studiekonsultasjon ved RH, hvor det skal gjøres klinisk undersøkelse, spørreskjemaer (SF-36 og HAQ), biobanking (blod, urin, avføring) og bildeundersøkelser (UL, MR og/eller PET)
64 pasienter er fra tidligere inkludert i NOSVAR. Vi planlegger en strategi for å finne ytterligere pasienter i Helse Sør-øst, samt pasienter i andre helseregioner.
Pasienter som allerede er inkludert i NOSVAR vil tilsendes et informasjonsskriv om studien. Siden de allerede er inkludert i NOSVAR vil de automatisk inkluderes i Del 1 av studien.
Pasienter som ikke er inkludert i NOSVAR vil tilsendes et informasjonsskriv om studien og NOSVAR-samtykke. Pårørende av avdøde pasienter vil sendes et passivt samtykk Artikkel: Performance of the 2019 ACR/EULAR classification criteria and the 2020 Revised Comprehensive Diagnostic Criteria across phenotypes in a Norwegian IgG4-related disease (IgG4-RD) cohort forventes innsendt primo 2023.
GPA–Wegeners Genetikk studie på ANCA assosiert vaskulitt (Universitetet i Uppsala)
Prosjekt-tittel: ”Identifiering och funktionella studier av genetiska riskfaktorer för ANCA-associerade vaskuliter”.
Prosjektleder: Johanna Dahlqvist, Institutionen för medicinsk biokemi och mikrobiologi, Uppsala universitet. Medarbeider: dr. Med. Øyvind Palm, OUS.
REK sør-øst: 2009/128 Genetiske markører ved systemiske, autoimmune sykdommer.
Dette er et genetikk-samarbeidsprosjekt om ANCA assosierte vaskulitter mellom universitetssykehusene i Uppsala, Umeå, Linköping, Lund/Malmö, Karolinska sjukhuset i Solna/Huddinge og Revmatologisk seksjon Oslo Universitetssykehus, Rikshospitalet. Første resultater ble publisert i desember 2021: Identification and Functional Characterization of a Novel Susceptibility Locus for Small Vessel Vasculitis with MPO-ANCA. Dahlqvist J.Rheumatology (Oxford). 2021 Dec. Øyvind Palm og Hilde Haukeland er medforfattere.
Fibroserende lungesykdommer
Interstitiell lungesykdom ved bindevevssykdommer og leddgikt
Prosjektansvarlig: MD PhD Anna-Maria Hoffmann-Vold
Prosjektmedarbeider: MD Phuong Phuon Diep, lungeavdelingen RH, OUS, MD PhD Trond Mogens Aaløkken, radiologisk avd, RH, OUS, MD John Belperio (lungeavdeling), Grace Kim og Jonathan Goldin (radiologisk avdeling) UCLA (University of California), Los Angeles, USA
Rek sør øst: #187572 REK har også gitt dispensasjon fra regelen om å innhente aktivt samtykke for avdøde pårørende med revmatisk sykdom (bindevevssykdommer og leddgikt).
Longitudinell observasjonsstudie. Alle pasienter med bindevevs sykdommer og RA med ILD blir tilsett av revmatolog og lungelege, kartlagt med lunge funksjon og HRCT, pasient rapporterte utfallsmål (PROMs)prøver til NOSVAR og dyp neseprøve til analyse på UCLA ved baseline og 12 måneder. Alle pasienter blir registrert i NOSVAR.
Det planlegges å inkludere 150 CTD-ILD pasienter fra NOSVAR, hittil er 130 pasienter inkludert.
Moderne metoder for sykdomsoppfølging ved revmatologisk sykdom med lungepåvirkning.
Prosjektleder: Emily Langballe (MD, PhD-kandidat)
Prosjektmedarbeider (veiledere): MD PhD Anna-Maria Hoffmann Vold og Øyvind Molberg (MD, professor)
REK: 535561 pr 16.11.22
Lungesykdom ved revmatologisk sykdom kan oppføre seg uforutsigbart og være både mild og alvorlig. Likevel blir slike sykdommer ofte behandlet likt i kliniske studier, da man ikke har noen god metode for å plukke ut pasienter som har dårlig prognose. Dette påvirker kunnskapsgrunnlaget vedr. behandling av disse sjeldne sykdommene. I dette prosjektet ønsker vi å bruke data fra NOSVAR-registeret for å bli bedre kjent med hvordan disse sykdommene oppfører seg, og om vi kan gjenkjenne noen mønster. Vi vil deretter planlegge og gjennomføre en forskningsstudie som tar i bruk digital hjemmeoppfølging for å følge disse pasientene på en mer fleksibel måte, som kan være bedre tilpasset for individuelle sykdomsforløp. Målet er både at pasienter får hyppigere oppfølging med raskere reaksjon ved forverring, samt å minske unødvendige sykehusbesøk for pasienter med stabil sykdom, men også å kartlegg sykdomsoppførsel på gruppenivå på en mer detaljert måte. Med dette ønsker vi å bidra til at kunnskapsgrunnlaget i fremtiden blir bedre og mer individualisert.
OUS strategisk satsningsområde 2022-2027- Nye persontilpassede management strategier for fibroserende sykdommer
Prosjektleder: MD PhD Anna-Maria Hoffmann-Vold, Avdeling for revmatologi, hud- og infeksjonssykdommer, Klinikk for kirurgi, inflammasjonsmedisin og transplantasjon.
Medprosjektleder: Mona Elisabeth Rootwelt-Revheim, Avdeling for nukleærmedisin, Klinikk for radiologi og nukleærmedisin.
Dette strategiske forskningsområdet for utvikling av nye, persontilpassede management-strategier for fibroserende sykdommer etablerer et nytt og interdisiplinært miljø bestående av fagmiljøer fra fire klinikker ved Oslo universitetssykehus (revmatologi, kardiologi, nukleærmedisin/radiologi, bioinformatikk og statistikk.
Det vil bli utviklet og testet nye molekylære avbildningsteknikker, kliniske verktøy og nye biomarkører og integrere og implementere disse direkte i klinisk praksis. Dermed vil vi utvikle persontilpassete metoder innen diagnostikk, oppfølging og behandling for pasienter med fibroserende sykdommer. Dette vil muliggjøre svært konkurransedyktig translasjons- og klinisk forskning, som vil fremme igangsetting av nye kliniske studier, til fordel for pasienter med fibroserende sykdommer både lokalt, nasjonalt og internasjonalt. Pasienter fra NOSVAR inkluderes i testingen.
Persontilpassede metoder innen diagnostikk, oppfølging og behandling: Samarbeid på tvers av miljøer/convergence
Prosjektleder: Mona Elisabeth Rootwelt-Revheim, Avdeling for nukleærmedisin, Klinikk for radiologi og nukleærmedisin.
Medprosjektleder: MD PhD Anna-Maria Hoffmann-Vold, Avdeling for revmatologi, hud- og infeksjonssykdommer, Klinikk for kirurgi, inflammasjonsmedisin og transplantasjon.
Hensikten er å utvikle persontilpassete metoder innen diagnostikk, oppfølging og behandling for pasienter med fibroserende sykdommer. Her vil utvikling av effektive kommunikasjonsstrategier mellom pasienten og helsepersonell fra diagnosetidspunkt og senere i forløpet være et viktig satsningsområde med mål om å etablere et mer bærekraftig pasientforløp. NOSVAR pasienter inkluderes.
ATHENA studien i oppdrag av Prometheus
REK og SLV godkjent, studien ferdig satt opp. Det planlegges å rekruttere 3-5 pasienter med SSc-ILD fra NOSVAR.
Nor-mILDer home monitoring strategy trial of CTD-ILD, start estimated May 2023
Myositter/Sjøgren/SLE
Genetiske markører ved systemiske, autoimmune sykdommer (Dissect studien), Universitetet i Uppsala, SVERIGE
Prosjektansvarlig: prof. dr. med. Øyvind Molberg
Prosjektmedarbeidere: Seksjon for revmatologi, OUS: dr.med Øyvind Palm, dr. med. Helena Andersson, MD PhD Karoline Lerang, Universitetet i Uppsala: Lars Rönnblom, Johanna Sandling
Rek sør-øst: 2016/685 Genetiske markører ved systemiske, autoimmune sykdommer.
DISSECT-studien er et Astra Zeneca (AZ)-Scilifelab-nordisk myositt samarbeidsprosjekt under ledelse av Professor Lars Rönnblom ved universitetet i Uppsala. Hensikten er å kartlegge koblingen mellom genetiske variasjon, immunologiske avvik og kliniske symptom ved tre ulike systemiske autoimmune sykdommer; SLE, Sjøgrens syndrom og myositt. Prosjektkoordinator er Johanna Sandling. DNA fra 155 myositt-pasienter fra NOSVAR biobanken ble inkludert i 2015. Serum fra de samme pasientene ble sendt i mai 2016. I 2017 er det i tillegg utlevert 143 EDTA av Sjøgren pasienter. Uttak er også gjort på 400 EDTA SLE som ble sendt i januar 2018. I mars 2019 ble samarbeidsprosjektet med Astra Zeneca (AZ)-Scilifelab avsluttet. Totalt 22 vitenskapelige publikasjoner (artikler og abstracts) er publisert i løpet av samarbeidsperioden. Data vil fortsatt bli analysert av Dissect akademia og flere studier er pågående. En artikkel med data fra pasienter inkludert i NOSVAR (Sjøgren) ble publisert i 2020.
For tiden arbeides med to publikasjoner. Et materiale er basert på 3.232 pasienter og over 17.000 europeiske kontroller. Primær internasjonal kontakt er Christopher J. Lessard ved Genes and Human Disease Research Program, Oklahoma Medical Research Foundation. En publikasjon som venter på å bli publisert: “Genome-wide association study of Sjögren disease identifies ten risk loci with potential functional implications in immune system and salivary gland».
Et annet manuscript “Complement C4 copy number variation is linked to SSA/SSB autoantibodies in systemic inflammatory autoimmune diseases”, et resultat av samarbeid med blant andre Christian Lundtoft ved Department of Medical Sciences, Rheumatology, Uppsala University. Øyvind Molberg, Helena Andersson og Øyvind Palm er som del av The DISSECT consortium medforfattere for NOSVAR. Studien omfatter gen-analyser av skandinaviske pasienter med SLE, Sjögrens syndrom eller myositt og friske kontroller ble publisert i 2022.
Påvisning av nye auto-antistoffer ved systemisk bindevevssykdommer
Prosjektleder: Forsker Fridtjof Lund–Johansen, Avdeling for immunologi og transfusjonsmedisin
Prosjektmedarbeidere: prof. dr. med Øyvind Molberg
Rek sør-øst: 2018/674 Utfallsrelaterte biomarkører ved systemiske inflammatoriske revmatiske sykdommer
Flere hundre selskaper verden over konkurrerer i dag om å selge over en million forskjellige antistoffer til forskere og diagnostiske laboratorier. Mange er av dårlig kvalitet, og binder ikke de proteiner de er laget for. Hensikten med denne studien er å finne ut om ny teknologi kan hjelpe oss til å identifisere flere auto antistoffer ved systemiske bindevevs sykdommer på tvers av diagnosene SLE, MCTD og SSc. Undersøkelsen av ulike serum bestanddeler gjennomføres ved hjelp av egnet undersøkelsesmetodikk (ELISA, multiplex assays og proteomikk-baserte assays) og (2) karakterisering av immunkompetente celler fra blod ved hjelp av overflatemarkør-analyser og biokjemiske undersøkelser. Artikkelskriving pågår
Identifisering av potensielle patogene T-celler fra blod fra pasienter med systemisk sklerose og SLE
Prosjektleder: Postdoc Asbjørn Christophersen, Immunologisk institutt, OUS
Prosjektmedarbeider: prof. dr. med. Øyvind Molberg
Rek sør-øst: 2018/674 Utfallsrelaterte biomarkører ved systemiske inflammatoriske revmatiske sykdommer. Ferske blodprøver av SSc og SLE pasienter inkludert i NOSVAR ble levert til analyse m/massecytometri som kan identifisere over 40 overflatemarkører på celler. Prosjektet er et samarbeid mellom Immunologisk institutt og Stanford University, California. Den første artikkelen fra prosjektet er under revisjon i et svært prestisjetungt tidsskrift.
Genuttrykk i isolerte B-celler
Prosjektleder: Postdoc Rasmus Iversen, Immunologisk institutt
Samarbeidspartner: prof. dr. med. Øyvind Molberg
REK sør-øst:
2018 ble det levert ferske celler fra 10 pasienter i NOSVAR. Isolerte B-lymfocytter ble sendt til USA for analyse av genutrykket i enkeltceller. En ny oppfølging med 10 nye pasienter blir utført i 2019. Artikkel publisert i 2022.
Disputaser/mastergrad
Ingen disputaser ble avholdt i 2022.
Sykepleier Mona-Lovise Talaro Ramsli leverte og fikk bestått på sin master med tittel: «The nurses contribution to quality of life in systemic sclerosis and proven pulmonary arterial hypertension, -a study based on patients experiences and thoughts in meeting with nurses in their treatment within the specialist health care in Norway.”
Samarbeid med andre registre
European scleroderma and research group
Data fra NOSVAR-pasienter med Systemisk sklerose inngår i det store felleseuropeiske forskningsnettverket European Scleroderma Trial and Research group (EUSTAR: http://www.eustar.org/ ). Nettverket har fokus på epidemiologi og nye behandlingsformer. Vi bidrar med data som er tiltenkt å føre til bedrede fremtidige behandlingsmuligheter.
MyoNet
Samarbeid om myositter, både epidemiologiske aspekter og prosjekter mer rettet mot sykdomsmekanismer gjøres gjennom vår deltagelse i EuMyoNet (http://myonet.eu/about-us/what-is-eumyonet/).
Publikasjoner med bidrag fra Nosvar og biobank i 2022
Totalt 31 publikasjoner med data fra register og RHI biobank er publisert i 2022. Studiene er gjort på følgende diagnoser; Systemisk sklerose (25), SLE (1), Myositter (1), Sjøgren (2) og vaskulitter (2). Antallet publikasjoner i perioden 2010-2022 er vist i figur 3.
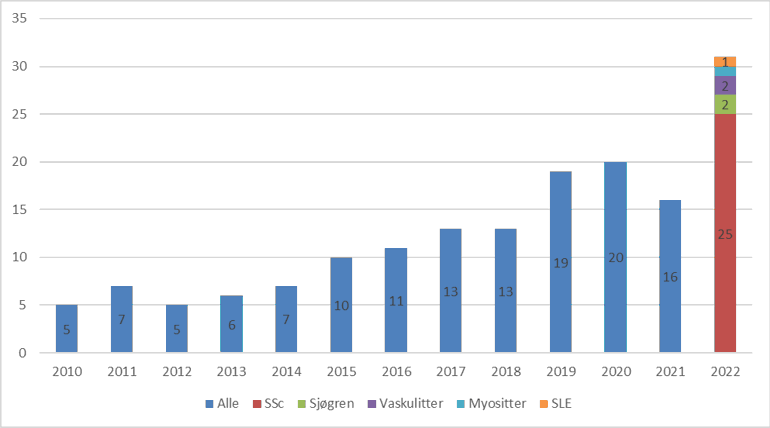
Publikasjoner i 2022: Systemisk sklerose
- Bruni C, Chung L, Hoffmann-Vold AM, Assassi S, Gabrielli A, Khanna D, Bernstein EJ, Distler O, EUSTAR and SCTC collaborators (2022)
High-resolution computed tomography of the chest for the screening, re-screening and follow-up of systemic sclerosis-associated interstitial lung disease: a EUSTAR-SCTC survey. Clin Exp Rheumatol, 40 (10), 1951-1955
DOI 10.55563/clinexprheumatol/7ry6zz, PubMed 35819810 Cristin 2081317 (Details) - Bruni C, Heidenreich S, Duenas A, Hoffmann-Vold AM, Gabrielli A, Allanore Y, Chatelus E, Distler JHW, Hachulla E, Hsu VM, Hunzelmann N, Khanna D, Truchetet ME, Walker UA, Alves M, Schoof N, Saketkoo LA, Distler O (2022). Patient preferences for the treatment of systemic sclerosis-associated interstitial lung disease: a discrete choice experiment. Rheumatology (Oxford), 61 (10), 4035-4046. DOI 10.1093/rheumatology/keac126, PubMed 35238334 Cristin 2077563 (Details)
-
Campochiaro C, Hoffmann-Vold AM, Avouac J, Henes J, de Vries-Bouwstra J, Smith V, Siegert E, Airò P, Oksel F, Pellerito R, Vanthuyne M, Pozzi MR, Inanc M, Sibilia J, Gabrielli A, Distler O, Allanore Y, (2022). Sex influence on outcomes of patients with systemic sclerosis-associated interstitial lung disease: an EUSTAR database analysis. Rheumatology (Oxford) (in press)
DOI 10.1093/rheumatology/keac660, PubMed 36413079 (Details) -
Didriksen H, Molberg Ø, Mehta A, Jordan S, Palchevskiy V, Fretheim H, Gude E, Ueland T, Brunborg C, Garen T, Midtvedt Ø, Andreassen AK, Lund-Johansen F, Distler O, Belperio J, Hoffmann-Vold AM (2022). Target organ expression and biomarker characterization of chemokine CCL21 in systemic sclerosis associated pulmonary arterial hypertension. Front Immunol, 13, 991743. DOI 10.3389/fimmu.2022.991743, PubMed 36211384 Cristin 2078795(Details)
-
Garaiman A, Steigmiller K, Gebhard C, Mihai C, Dobrota R, Bruni C, Matucci-Cerinic M, Henes J, de Vries-Bouwstra J, Smith V, Doria A, Allanore Y, Dagna L, Anić B, Montecucco C, Kowal-Bielecka O, Martin M, Tanaka Y, Hoffmann-Vold AM, Held U, Distler O, Becker MO, (2022). Use of platelet inhibitors for digital ulcers related to systemic sclerosis: EUSTAR study on derivation and validation of the DU-VASC model. Rheumatology (Oxford) (in press)
DOI 10.1093/rheumatology/keac405, PubMed 35904554 (Details) -
Hilberg O, Hoffmann-Vold AM, Smith V, Bouros D, Kilpeläinen M, Guiot J, Morais A, Clemente S, Daniil Z, Papakosta D, Fretheim H, Neves S, Alfaro TM, Antoniou KM, Valveny N, Asijee G, Soulard S, Wuyts W (2022). Epidemiology of interstitial lung diseases and their progressive-fibrosing behaviour in six European countries. ERJ Open Res, 8 (1). DOI 10.1183/23120541.00597-2021, PubMed 35083316 Cristin 2031129 (Details)
-
Hoffmann-Vold AM, Brunborg C, Airò P, Ananyeva LP, Czirják L, Guiducci S, Hachulla E, Li M, Mihai C, Riemekasten G, Sfikakis P, Valentini G, Kowal-Bielecka O, Allanore Y, Distler O (2022). Cohort Enrichment Strategies for Progressive Interstitial Lung Disease in Systemic Sclerosis From European Scleroderma Trials and Research. Chest (in press). DOI 10.1016/j.chest.2022.09.044, PubMed 36244404 (Details)
-
Hoffmann-Vold AM, Distler O, Bruni C, Denton CP, de Vries-Bouwstra J, Matucci Cerinic M, Vonk MC, Gabrielli A (2022). Systemic sclerosis in the time of COVID-19. Lancet Rheumatol, 4 (8), e566-e575
DOI 10.1016/S2665-9913(22)00130-8, PubMed 35891634 Cristin 2044896 (Details) -
Hoffmann-Vold AM, Distler O, Crestani B, Antoniou KM (2022)
Recent advances in the management of systemic sclerosis-associated interstitial lung disease. Curr Opin Pulm Med, 28 (5), 441-447
DOI 10.1097/MCP.0000000000000901, PubMed 35855572 Cristin 2047666 (Details) -
Hughes M, Huang S, Alegre-Sancho JJ, Carreira PE, Engelhart M, Hachulla E, Henes J, Kerzberg E, Pozzi MR, Riemekasten G, Smith V, Szücs G, Vanthuyne M, Zanatta E, Distler O, Gabrielli AG, Hoffmann-Vold AM, Steen VD, Khanna D, (2022). Late Skin Fibrosis in Systemic Sclerosis: A Study from the EUSTAR Cohort. Rheumatology (Oxford) (in press)
DOI 10.1093/rheumatology/keac363, PubMed 35731139 (Details) -
Iudici M, Jarlborg M, Lauper K, Müller-Ladner U, Smith V, Allanore Y, Balbir-Gurman A, Doria A, Airò P, Walker UA, Riccieri V, Vonk MC, Gabrielli A, Hoffmann-Vold AM, Szücs G, Martin T, Distler O, Courvoisier DS, EUSTAR collaborators (2022). Representativeness of systemic sclerosis patients in interventional randomized trials: an analysis of the EUSTAR database.
Rheumatology (Oxford), 61 (2), 743-755. DOI 10.1093/rheumatology/keab437, PubMed 33989387 Cristin 2025848 (Details) -
Iudici M, Mongin D, Siegert E, Carreira PE, Distler J, Henes J, Zanatta E, Hachulla E, De Luca G, Müller CS, Santiago T, Tandaipan JL, Bianchi BV, De Santis M, Hoffmann-Vold AM, Gabrielli A, Distler O, Courvoisier DS, (2022). Glucocorticoids prescribing practices in systemic sclerosis: an analysis of the EUSTAR database. Rheumatology (Oxford) (in press)
DOI 10.1093/rheumatology/keac533, PubMed 36099040 (Details) -
Kreuter M, Hoffmann-Vold AM, Matucci-Cerinic M, Saketkoo LA, Highland KB, Wilson H, Alves M, Erhardt E, Schoof N, Maher TM (2022). Impact of lung function and baseline clinical characteristics on patient-reported outcome measures in systemic sclerosis-associated interstitial lung disease. Rheumatology (Oxford) (in press)
DOI 10.1093/rheumatology/keac325, PubMed 35640959 (Details) -
Kuster S, Jordan S, Elhai M, Held U, Steigmiller K, Bruni C, Cacciapaglia F, Vettori S, Siegert E, Rednic S, Codullo V, Airo P, Braun-Moscovici Y, Hunzelmann N, Joao Salvador M, Riccieri V, Gheorghiu AM, Alegre Sancho JJ, Romanowska-Prochnicka K, Castellví I, Kötter I, Truchetet ME, López-Longo FJ, Novikov PI, Giollo A et al. (2022). Effectiveness and safety of tocilizumab in patients with systemic sclerosis: a propensity score matched controlled observational study of the EUSTAR cohort. RMD Open, 8 (2). DOI 10.1136/rmdopen-2022-002477, PubMed 36328401 Cristin 2085583 (Details)
-
Lescoat A, Huscher D, Schoof N, Airò P, de Vries-Bouwstra J, Riemekasten G, Hachulla E, Doria A, Rosato E, Hunzelmann N, Montecucco C, Gabrielli A, Hoffmann-Vold AM, Distler O, Ben Shimol J, Cutolo M, Allanore Y, (2022)
Systemic sclerosis-associated interstitial lung disease in the EUSTAR database: analysis by region. Rheumatology (Oxford) (in press)
DOI 10.1093/rheumatology/keac576, PubMed 36222557 (Details) -
Matteson EL, Kelly C, Distler JHW, Hoffmann-Vold AM, Seibold JR, Mittoo S, Dellaripa PF, Aringer M, Pope J, Distler O, James A, Schlenker-Herceg R, Stowasser S, Quaresma M, Flaherty KR, INBUILD Trial Investigators (2022). Nintedanib in Patients With Autoimmune Disease-Related Progressive Fibrosing Interstitial Lung Diseases: Subgroup Analysis of the INBUILD Trial. Arthritis Rheumatol, 74 (6), 1039-1047
DOI 10.1002/art.42075, PubMed 35199968 Cristin 2062094 (Details) -
Roofeh D, Brown KK, Kazerooni EA, Tashkin D, Assassi S, Martinez F, Wells AU, Raghu G, Denton CP, Chung L, Hoffmann-Vold AM, Distler O, Johannson KA, Allanore Y, Matteson EL, Kawano-Dourado L, Pauling JD, Seibold JR, Volkmann ER, Walsh SLF, Oddis CV, White ES, Barratt SL, Bernstein EJ, Domsic RT et al. (2022). Systemic Sclerosis Associated Interstitial Lung Disease: A Conceptual Framework for Subclinical, Clinical, and Progressive Disease. Rheumatology (Oxford) (in press)
DOI 10.1093/rheumatology/keac557, PubMed 36173318 (Details) -
Schniering J, Maciukiewicz M, Gabrys HS, Brunner M, Blüthgen C, Meier C, Braga-Lagache S, Uldry AC, Heller M, Guckenberger M, Fretheim H, Nakas CT, Hoffmann-Vold AM, Distler O, Frauenfelder T, Tanadini-Lang S, Maurer B (2022). Computed tomography-based radiomics decodes prognostic and molecular differences in interstitial lung disease related to systemic sclerosis. Eur Respir J, 59 (5). DOI 10.1183/13993003.04503-2020, PubMed 34649979 Cristin 2047249 (Details)
-
Tennøe AH, Murbræch K, Didriksen H, Ueland T, Palchevskiy V, Weigt SS, Fretheim H, Midtvedt Ø, Garen T, Brunborg C, Aukrust P, Molberg Ø, Belperio JA, Hoffmann-Vold AM (2022). Serum markers of cardiac complications in a systemic sclerosis cohort. Sci Rep, 12 (1), 4661
DOI 10.1038/s41598-022-08815-8, PubMed 35304587 Cristin 2017203 (Details) -
Volkmann ER, Kreuter M, Hoffmann-Vold AM, Wijsenbeek M, Smith V, Khanna D, Denton CP, Wuyts WA, Miede C, Alves M, Sambevski S, Allanore Y (2022)
Dyspnoea and cough in patients with systemic sclerosis-associated interstitial lung disease in the SENSCIS trial. Rheumatology (Oxford), 61 (11), 4397-4408. DOI 10.1093/rheumatology/keac091, PubMed 35150246 Cristin 2087559 (Details) -
Wang Y, Xie X, Zheng S, Du G, Chen S, Zhang W, Zhuang J, Lin J, Hu S, Zheng K, Mikish A, Xu Z, Zhang G, Gargani L, Bruni C, Hoffmann-Vold AM, Matucci-Cerinic M, Furst DE (2022). Serum B-cell activating factor and lung ultrasound B-lines in connective tissue disease related interstitial lung disease. Front Med (Lausanne), 9, 1066111. DOI 10.3389/fmed.2022.1066111, PubMed 36590969 Cristin 2107402(Details)
-
Zanatta E, Huscher D, Ortolan A, Avouac J, Airò P, Balbir-Gurman A, Siegert E, Matucci Cerinic M, Cozzi F, Riemekasten G, Hoffmann-Vold AM, Distler O, Gabrielli A, Heitmann S, Hunzelmann N, Montecucco C, Morovic-Vergles J, Ribi C, Doria A, Allanore Y, EUSTAR collaborators (2022). Phenotype of limited cutaneous systemic sclerosis patients with positive anti-topoisomerase I antibodies: data from the EUSTAR cohort. Rheumatology (Oxford), 61 (12), 4786-4796. DOI 10.1093/rheumatology/keac188, PubMed 35348643 Cristin 2094351 (Details)
-
Campochiaro C, Hoffmann-Vold AM, Avouac J, Henes J, de Vries-Bouwstra J, Smith V, Siegert E, Airò P, Oksel F, Pellerito R, Vanthuyne M, Pozzi MR, Inanc M, Sibilia J, Gabrielli A, Distler O, Allanore Y; EUSTAR collaborators. Sex influence on outcomes of patients with systemic sclerosis-associated interstitial lung disease: an EUSTAR database analysis. Rheumatology (Oxford). 2022 Nov 22:keac660.
-
Hoffmann-Vold AM, Volkmann ER, Allanore Y, Assassi S, de Vries-Bouwstra JK, Smith V, Tschoepe I, Loaiza L, Kanakapura M, Distler O. Safety and tolerability of nintedanib in patients with interstitial lung diseases in subgroups by sex: a post-hoc analysis of pooled data from four randomised controlled trials. The Lancet Rheumatol 2022, Oct e679-e687
-
Truchetet ME, López-Longo FJ, Novikov PI, Giollo A, Shirai Y, Belloli L, Zanatta E, Hachulla E, Smith V, Denton C, Ionescu RM, Schmeiser T, Distler JHW, Gabrielli A, Hoffmann-Vold AM, Kuwana M, Allanore Y, Distler O; EUSTAR collaborators. Effectiveness and safety of tocilizumab in patients with systemic sclerosis: a propensity score matched controlled observational study of the EUSTAR cohort. RMD Open. 2022 Nov;8(2):e002477.
Publikasjoner i 2022: SLE, Sjøgren, myositter
- Hynne H, Aqrawi LA, Jensen JL, Thiede B, Palm Ø, Amdal CD, Westgaard KL, Herlofson BB, Utheim TP, Galtung HK (2022). Proteomic Profiling of Saliva and Tears in Radiated Head and Neck Cancer Patients as Compared to Primary Sjögren's Syndrome Patients. Int J Mol Sci, 23 (7). DOI 10.3390/ijms23073714, PubMed 35409074 Cristin 2024351 (Details)
- Mariette X, Barone F, Baldini C, Bootsma H, Clark KL, De Vita S, Gardner DH, Henderson RB, Herdman M, Lerang K, Mistry P, Punwaney R, Seror R, Stone J, van Daele P, van Maurik A, Wisniacki N, Roth DA, Tak PP (2022). A randomized, phase II study of sequential belimumab and rituximab in primary Sjögren's syndrome. JCIInsight, 7 (23). DOI 10.1172/jci.insight.163030, PubMed 36477362 Cristin 2097786 (Details)
- Lundtoft C, Pucholt P, Martin M, Bianchi M, Lundström E, Eloranta ML, Sandling JK, Sjöwall C, Jönsen A, Gunnarsson I, Rantapää-Dahlqvist S, Bengtsson AA, Leonard D, Baecklund E, Jonsson R, Hammenfors D, Forsblad-d'Elia H, Eriksson P, Mandl T, Magnusson Bucher S, Norheim KB, Auglaend Johnsen SJ, Omdal R, Kvarnström M, Wahren-Herlenius M et al. (20 Anderson H, Molberg Ø, medforfattere). Complement C4 Copy Number Variation is Linked to SSA/Ro and SSB/La Autoantibodies in Systemic Inflammatory Autoimmune Diseases. Arthritis Rheumatol, 74 (8), 1440-1450
DOI 10.1002/art.42122, PubMed 35315244 Cristin 2065345 (Details) - Rothwell S, Amos CI, Miller FW, Rider LG, Lundberg IE, Gregersen PK, Vencovsky J, McHugh N, Limaye V, Selva-O'Callaghan A, Hanna MG, Machado PM, Pachman LM, Reed AM, Molberg Ø, Benveniste O, Mathiesen P, Radstake T, Doria A, De Bleecker JL, De Paepe B, Maurer B, Ollier WE, Padyukov L, O'Hanlon TP et al. (2022). Genome-wide imputation identifies novel associations and localises signals in idiopathic inflammatory myopathies. Arthritis Rheumatol (in press). DOI 10.1002/art.42434, PubMed 36580032 (Details)
Publikasjoner i 2022: Vaskulitter
- Dahlqvist J, Ekman D, Sennblad B, Kozyrev SV, Nordin J, Karlsson Å, Meadows JRS, Hellbacher E, Rantapää-Dahlqvist S, Berglin E, Stegmayr B, Baslund B, Palm Ø, Haukeland H, Gunnarsson I, Bruchfeld A, Segelmark M, Ohlsson S, Mohammad AJ, Svärd A, Pullerits R, Herlitz H, Söderbergh A, Rosengren Pielberg G, Hultin Rosenberg L et al. (2022). Identification and functional characterization of a novel susceptibility locus for small vessel vasculitis with MPO-ANCA. Rheumatology (Oxford), 61 (8), 3461-3470. DOI 10.1093/rheumatology/keab912, PubMed 34888651 Cristin 2006924 (Details)
- Zeng L, Walsh M, Guyatt GH, Siemieniuk RAC, Collister D, Booth M, Brown P, Farrar L, Farrar M, Firth T, Fussner LA, Kilian K, Little MA, Mavrakanas TA, Mustafa RA, Piram M, Stamp LK, Xiao Y, Lytvyn L, Agoritsas T, Vandvik PO, Mahr A (2022). Plasma exchange and glucocorticoid dosing for patients with ANCA-associated vasculitis: a clinical practice guideline. BMJ, 376, e064597
DOI 10.1136/bmj-2021-064597, PubMed 35217581 (Details)
Presenterte registerdata på kongresser
EULAR (European Alliance of associations for rheumatology) Copenhagen 2022
- High levels of both CCL2 and CCL17 were associated with more severe SSc-ILD, Barua1, et al.
- Patients with systemic sclerosis have impared forced vital capacity, even in the absence of interstitial lung disease, Fretheim1, et al.
- Risk stratification approaches perform differently in SSc-associated PAH in EUSTAR, J. Bjørkekjær1 et al.
- Interstitial lung disease associated with primary sjøren syndrome is frequently progressive, A. M. Hoffmann-Vold1 et al.
- Progressive interstitial lung disease is frequent also in late disease stages in systemic sclerosis patients from EUSTAR, A M. Hoffmann-Vold1 et al.
- Phenotypes and disease characteristics of IgG4-related disease in Norway, Vikse1,2 et al.
- Working and health status in Norwegian patients with Takayasu arteritis, T.Garen 1 et al
1 Oslo University hospital, Rheumatology, Oslo, Norway
2 University of Bergen, Clinical Science, Bergen, Norway
ACR (American Congress of Rheumatology), Annual meeting, E-congress, Philadelphia, USA, nov 2022
- Rituximab in IgG4-Related Diseae: An Open-Label Non-Randomized Observational Study, Jens Vikse1 et al
- The 2019 ACR/EULAR Classification Criteria for IgG4-Related Disease Perform Lower Than Expected: Data from a Norwegian Cohort, Jens Vikse1 et al
- The Role of CCL21 in Serum Samples from Systemic Sclerosis Patients, Henriette Didriksen1 et al
- Patients with Systemic Sclerosis Have Impaired Forced Vital Capacity, Even in the Absence of Interstitial Lung Disease, Håvard Fretheim1 et al
- Risk Stratification of Patients with Systemic Sclerosis-associated Pulmonary Arterial Hypertension in EUSTAR Using the Current and New Proposed Criteria, Hilde Jenssen Bjørkekjær1 et al
- Discordance of Patient, Physician and Nurse Practitioner Assessment of Disease Burden in Systemic Sclerosis, Maylen Nordgård Carstens1 et al
- The Role of CCL21 in Serum Samples from Systemic Sclerosis Patients, Henriette Didriksen1 et al
1 Oslo University hospital, Rheumatology, Oslo, Norway
2 University of Bergen, Clinical Science, Bergen, Norway
Oral presentation at the Nordic PH forum 2022
Bjørkekjær HJ, Bruni C, Carreira P, Airò P, Aznar CPS, Truchetet ME, Giollo A, Balbir-Gurman A, Martin M, Denton CP, Gabrielli A, Fretheim H, Barua I, Bitter H, Midtvedt Ø, Broch K, Andreassen A, Tanaka Y, Riemekasten G, Müller-Ladner U, Matucci-Cerinic M, Castellví I, Siegert E, Hachulla E, Distler O, Hoffmann-Vold AM. Risk Stratification of Patients with Systemic Sclerosis-associated Pulmonary Arterial Hypertension in EUSTAR Using the New Definition of Pulmonary Hypertension.
Mål for 2023
- Fortsatt arbeide for å øke antallet inkluderte pasienter med sikker diagnose.
- Opprettholde rutiner for blodprøvetaking innenfor økonomiske rammer og kvotebegrensningen.
- Bedre rutiner for komplett utfylte registreringsskjema.
- Gjennomføre planlagte utvidelser av NOSVAR.
- Legge til rette for fortsatt nasjonalt- og internasjonalt samarbeid.
Utfordringer i 2023
Registeret er avhengig av litt mer midler for å nå målsettingen for 2023. Spesielt gjeldet det å kunne dekke kostandene ved målet om mer biobanking/prøvetaking av alle pasienter til RHI biobanken og planlagte utvidelser av NOSVAR.